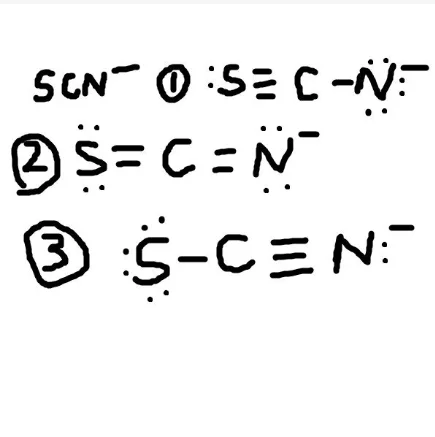
将键合电子的半数分别归属各键合原子,再加上各原子的孤电子数,如果两者之和等于该原子(成游离态电中性时)的价层电子数,形式电荷来自记为零,否则,少了电子,形式电荷记"+"数,多了电子记为"-"数。
形式电荷是在写360百科共价化合物的Lewis结构式时为了判断各可能物种的稳定性时引入的。
其大小等于价电子数-(成键后)实际拥有价电子数。如季铵盐,共振式中常见到的正负号,在无机中,如用分子轨道理论处理CO后,C:形式电荷=4沿做紧粮-(2+3)=-1;O:形式电荷=6-(2+3)=+1.
再举一例,如判断共振八隅体稳定性:首先形式电荷越接近0越稳定,其次形式电荷正负交替时最稳定。
- 中文名 形式电荷
- 外文名 formal charges
- 学科 化学
- 性质 共价化合物
- 判断 稳定性
计算方法
形式电荷q=原子价电子数-键数-孤电子数
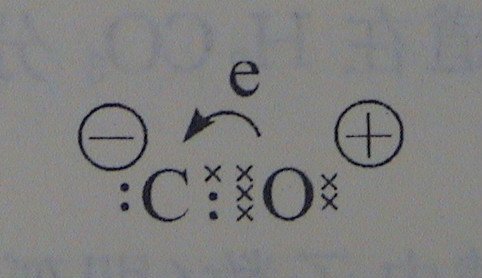 形式电荷
形式电荷 例:CO分子中,q(C)=4-3-2=-1
与Lewis的结构
形式电荷可以用来判断所写的Lewis结构是否合理。例如:SCN1- 的 Lewis结构应该是将碳原子放在中间,氮原子和硫原子分别放在两边。此时,硫原子的形式电荷是-1,碳原子和氮原子的个校象员北形式电荷是0;但如果将硫原子安排在中间,则氮原子的形式电荷是-1,碳原子的形式电荷是-2,硫原子的形式电荷是+2。可以看出,后者中,各原子形式电荷数相差很多,结构不稳定,显然前者更合理。
 形式电荷
形式电荷
根据判断Lewi成敌述移顺s结构式的稳定性
⑴在Lewis结构式中,q应尽量小,若共价分子中所有原子的形式电荷都为零,则是最稳定的Lewis结构式;
 形式看电荷
形式看电荷 ⑵两相邻原子之间的形式电荷应避免同号。
版权声明:此文信息来源于网络,登载此文只为提供信息参考,并不用于任何商业目的。如有侵权,请及时联系我们:sji1127@163.com


