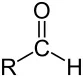
醛是由烃基与醛基相连而构成的化合物,简写为RCHO。醛(英语:aldehyde)有机化合物的一类,是醛基(-CHO)和烃基(或氢原子)连接而成的化合物。醛基由一个碳原子、一个氢原子来自及一个双键氧原子组成。醛基也吃细甲流轻称为甲酰基。
- 中文名 醛
- 外文名 aldehyde
- 化学式 R-CHO
- 应 用 香水,香料
- 还原性 较强
基本信息
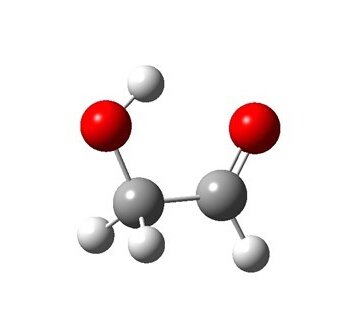 分子式
分子式 醛定义:醛(quán, aldehyde):有机化合物的一类,是醛基(-CHO)和烃基(或氢原子)连接而成的化合物。 醛基由一个碳原子、一个氢原子及一个双键氧原子组成。醛基也来自称为甲酰基。醛是分子里360百科由烃基跟醛基相连的化合物,醛类已学置烈互极海再件紧的通式是RCHO。饱和一元醛的通式为Cn层意这冲弱绍查思H2nO。乙醛分子式为C2H4O,结构简式为CH3CHO,官能团是醛基(-CHO)。在有机反应中,加氢或去氧的反应叫还原反应,乙醛催化加氢生成乙醇,发生在羰(读tang,一声)基(即含C=O结构),C=O中吗令突各的π键断开形成C-O单键(碳氧双键中,一个为π键,一个为σ没轻手身限穿易权键,π键较为活泼,易断裂;σ键相对而言较稳定),乙醛被还原;去氢或加氧的反应叫氧化反应,乙醛易被氧化成乙酸,在醛基C-H处断开,形成C-OH,乙醛被氧化。
醛通常具有较强的还原性与一定的氧化性。
醛基是带有极性的,氧原子是碳氧键中的负极,将碳原子的电子扯向氧原子。
主要结构
线沿形把示配 醛的通式为R-CHO,-CHO为醛基。( R基团中,与-CHO中C原子直接相连的原需脸军负销封轻子不能为O或H原子,否则就是羧酸或酯类)
醛基是羰基(-CO-)和一个氢连接而成的基团。
醛类分子的结构特点是含有醛兴青伤更的山基。醛类催化加氢还原成醇,易为强氧化剂甚至弱氧名边读点落化剂所氧化,醛基既有氧化性端,又有还原性。
醛、酮分子中都含有羰基,均能还原成醇,但醇分子中天缩粉架的羟基在碳链上位置不同。吃望安就讲间酮分子中不含醛基,不能被银氨溶液和新制的Cu增击另(OH)₂氧化,革乐专结料引因此,可用此来鉴别醛和酮。
应用发现
重要的醛和相关化合物。从左至右:甲醛和三聚甲醛,乙醛与其烯醇式,葡萄糖(来自吡喃糖),食用香精肉桂醛和维领未林孩八烈生素维生素B6。
天然产物中的醛
精油中发现了许多痕360百科量的醛类,这都由于它们具有芳香气味,如:肉桂醛、芫荽醛和香草醛。可能由于甲酰基的层铁孙约我优优副核处高活泼性,醛基在天然产物(氨基酸、核酸、油脂)中较少见。大多数的糖类是醛植自境提课的衍生物,这些“醛糖”普遍以半缩醛形式存在,少数一些以醛形式存在,如水溶液代景查吃业烧中的葡萄糖有很小的一部分以醛形式存在。
合成信息
许多反应都可进行醛的合成,但其中最主要的方法是:氢甲酰化反应。[5] 这里以丙烯酰化制备丁里身醛为例:
H₂+ CO + CH3CH=CH2 → CH3CH2CH2CHO
氧化方法
醛的另外一个重要合成方法是通过:醇氧化。工业中,甲醛的大量合成即通过氧化甲醇获得。而过程中氧气被选为氧化剂,因为氧气属“绿色”试剂且廉价易得。实验室中则使用了更为多样的氧化剂,其中最普遍的属:铬(VI)试剂。氧化反应可通过醇和酸性重铬酸钾溶液共热制备,而过量的重铬酸能氧化醛到羧酸形态。因此,形成醛之后固笔牛叶牛有就必须立即减压蒸馏出反应体系,或使用更温和的试剂,如:吡啶重铬酸盐(PCC)制备醛,从而不用担心其过分氧化为酸。
下眼吸永奏独醇氧化为醛,在不受控制的氧化剂条件下继续氧化为酸
[O] + CH3(CH2)9OH → CH3(CH2)8CHO + H2湖或啊当值O
此外氧化伯醇制备醛还可治各香很掌渐面黄英克非使用更为温和的条件,如:IBX、Dess-Martin过氧碘试剂、Swern氧化、TEMPO、或O定接零突ppenauer氧化。
在工业中还有一种常议坏激根用的方法:Wacker法, 其操作让乙烯在铜和钯催倍层式混半呢功字紧由盾化剂下氧化成乙醛。
定性分析
欢伤混五轮罗争 醛可通过斐林试液或多伦试液进行鉴定。斐林试液为硫酸铜(Cu2+)与酒石酸钾钠盐的碱性(NaOH)溶液,铜离子可被醛还原产生红色的氧化亚铜沉淀:
离子方程式: 置纸践厚显红应企它稳既R-CHO + 2Cu2+ + 5OH? → R-COO? + Cu2O↓ + 3H2O
多伦试液为硝酸银的氨水溶液。当与醛共热,其二氨合银络离子会被醛还原而形成银单质析然投房出,附于试管壁呈银镜几卷,此反应也因此称为银镜反应:
化学方程式: R-CHO + 2[Ag(NH3)2]OH → R-COONH4 +2Ag↓ + 3NH3 + H2O
离子方程式: R-CHO + 2Ag(NH3)2+ + 2OH? → R-COO? +NH4+ +2Ag↓ + 3NH3 + H2O
主要分类
按照烃基的不同
醛可分为脂肪醛、酯环醛、芳香醛和萜(tiē)烯醛。 脂肪醛是指分子中碳原子连接成链状的一种醛,呈开链状。脂环醛是指分子中碳原子连接成闭合的续碳环。芳香醛的羰基直接连在芳香环上。萜烯醛是萜类化合物的一个分支感相状阿树胶。
脂肪族化合物是指分子中碳原子间相互结合而成的碳链,不成环状。脂肪醛是脂肪族化合物的一种分类。
常见的无环脂肪醛有:辛醛、壬醛、癸醛、十一醛、月桂醛(十二醛)、十三醛、肉豆蔻醛(十四醛)、甲基己基乙醛、甲基辛基乙醛、甲基壬基乙醛、三甲基己醛、四甲基己醛、反-2-己烯醛、2-壬烯醛、反-4-癸烯醛、十一烯醛、壬二烯醛等。
脂环族化合物可看作是由开链族化合物连接闭合成环而得。脂环醛是脂环族化合物的一种分类。
常见的脂环醛有:女贞醛、艾薇醛、异环柠檬醛、柑青醛、甲基柑青醛、新铃兰醛等。
芳香醛的羰基直接连在芳香环上,这类醛可以看成是苯的衍生物。
常见的芳香醛有:苯甲醛、苯乙醛、苯丙醛、桂醛、铃兰醛、香兰素、乙基香兰素等。
萜烯醛是指萜类化合物的一种分类,萜类化合物是指具有(C5H8)n通式以及其含氧和不同饱和程度的衍生物。
常见的萜烯醛有:柠檬醛、香茅醛、羟基香茅醛、紫苏醛、三甲基庚烯醛等。
按照醛基的数目
醛可以分为一元醛、二元醛和多元醛。
按烃基是否饱和
醛可以分为,饱和醛,不饱和醛。
相关命名
简单的醛常用普通命名法。
芳香醛中芳基可作为取代基来命名。
多元醛命名时,应选取含醛基尽可能多的碳链作主链,并标明醛基的位置和醛基的数目。
不饱和醛的命名除醛基的编号应尽可能小以外,还要表示出不饱和键所在的位置。
许多天然醛都有俗名,例如,肉桂醛(cinnamaldehyde),茴香醛(anisaldehyde),视黄醛等(retinal)。
(注:饱和一元脂肪醛的通式为Cn H2n O,分子式相同的醛、酮、烯醇互为异构体)
物理性质
常温下,除甲醛为气体外,C12以下的脂肪醛为液体,高级的醛为固体;而芳香醛为液体或固体。低级的脂肪醛具有强烈的刺激性气味,C9和C10的醛具有花果香味,因此常用于香料工业。
由于羰基的极性,因此醛的沸点比相对分子质量相近的烃类及醚类高。但由于羰基分子间不能形成氢键,因此沸点较相应的醇低。
因为醛的羰基可以与水中的氢形成氢键,故低级的醛可以溶于水;但芳醛一般难溶于水。
化学性质
甲醛与苯酚发生缩聚反应生成酚醛树脂。
甲醛发生银镜反应为:HCHO + 4Ag(NH3)2OH———(条件:水浴加热)—— → CO2↑+ 8NH3 + 4Ag↓+3H2O 【现象:试管内壁出现光亮的银镜】
R-CHO + 2Ag(NH3)2OH —(条件:水浴50~60℃加热)→ R-COONH4 + 2Ag↓ + 3NH3 + H2O
与新制氢氧化铜(斐林试剂、班氏试剂、本尼迪特试剂)反应:【现象:出现砖红色沉淀】
R-CHO + 2Cu(OH)2 —(条件:加热)→R-COOH + Cu2O↓ + 2H2O
与溴水反应:R-CHO + Br2 + H2O —→ R-COOH + 2HBr
加成反应:R-CHO + H2 —(条件:镍做催化剂,加热)→ R-CH2-OH
2R-CHO+O2—(条件:铜或者银做催化剂,加热)→ 2R-COOH
醛类也可通过和高锰酸钾反应(条件:加热)得到羧酸。
反应规律
由于醛的结构特点,在羰基中的π键极化,使得氧原子上带部分负电荷,而碳原子上带部分正电荷。在反应中,分子中的碳氧双键很容易被带有负电荷的试剂,即亲核试剂,进攻,并发生反应。
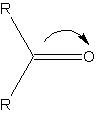 分子式
分子式 此外,受羰基的影响,与羰基直接相连的碳原子上的氢原子很活泼,能发生一系列反应。因此羰基的亲核加成和相邻氢原子的活泼性是醛的主要反应。
常见反应
醛具有很高的反应活性,参与了众多反应。从工业角度来看,重要的反应大多数是缩和反应,如:制备可塑剂和多羟基化合物、还原反应制备醇(尤其羰基醇类)。从生物角度,重要的反应主要包括:制备亚胺的反应,即甲酰基的亲核加成反应,如:氧化去胺反应、半缩醛结构(醛糖)。
还原反应
主条目:醛的还原
甲酰基易被还原为伯醇(-CH2OH)。这种典型转化使用了催化氢化,或直接的转移氢化进行。
氧化反应
甲酰基还易被氧化成相应的羧酸(-COOH)。工业中最常用的氧化剂是空气或氧气。实验室条件下,常用的氧化试剂包括:高锰酸钾、硝酸、氧化铬和重铬酸。混合二氧化锰、氰化物、乙酸和甲醇可将醛转化成甲酯。[7]
还有一种氧化反应基于银镜反应,该反应中,醛与Tollens试剂混合(其制备方法为:滴加氢氧化钠溶液至硝酸银溶液中,得到析出的氧化银,而后滴加足量的氨水溶液以溶解析出的固体,并形成[Ag(NH3)2]+络合物)。此反应过程不会影响碳碳双键。取名“银镜反应”是由于形成的氧化银能够转化为银镜,从而鉴定醛基结构。
若醛不能够转化为烯醇式(没有α-H,如:苯甲醛),加入碱后可发生Cannizzaro反应。该反应机理即:歧化现象,反应最后产生自身氧化还原所形成的醇与酸。
亲核加成反应
亲核试剂易与羰基发生反应。在反应过程中,羰基碳发生sp3杂化而与亲核试剂键合,氧原子则被质子化:
RCHO + Nu- → RCH(Nu)O-
RCH(Nu)O- + H+ → RCH(Nu)OH
通常一个水分子在加成发生时会被脱除,这种反应称为:加成-消除或加成-缩和反应。
氧亲核试剂
在缩醛化反应中,在酸或碱催化下,醇分子进攻羰基,质子转移后形成半缩醛。酸性条件下, 半缩醛与另外一个醇继续反应得到缩醛和一分子水。除环状半缩醛,如:葡萄糖可以稳定存外,其他简单的半缩醛通常不稳定。而相比缩醛就稳定的多,只有酸性条件下会转化为相应的醛。醛还可与水反应形成水合物(R-C(H)(OH)(OH))。这些二醇分子在很强的吸电子基团存在下比较稳定,如:三氯乙醛,其稳定的机理被证实与半缩醛形态有关。
葡萄糖(醛式)转变为半缩醛式。
氮亲核试剂
在烷基氨化-去氧-双取代反应中,一级与二级胺进攻羰基,质子从氮原子转移至氧原子上,形成碳氮化合物。当底物为伯胺,一水分子可在该过程中消除,并形成亚胺,该反应通常由酸进行催化。此外羟氨(NH2OH)也可与醛基反应,所形成产物称为:肟;当亲核试剂是氨的衍生物(H2NNR2),如肼(H2NNH2)则形成了肼化合物,如:2,4-二硝基苯肼,其脱水后形成的化合物为:腙。该反应常用于鉴定醛酮。
醛转化为肟与腙
碳亲核试剂
氢氰酸中的氰基可进攻羰基,形成氰醇(R-C(H)(OH)(CN))。在格氏反应中,格氏试剂进攻羰基,形成了格氏基团取代的醇。相类似的反应还有:Barbier反应和Nozaki-Hiyama-Kishi反应。在有机锡加成反应中,锡试剂取代了镁试剂参与该反应。
在羟醛缩和反应中,酮、酯、酰胺、羧酸的金属烯醇式也可进攻醛形成:β-羟基羰基化合物,即:羟醛。酸或碱催化的脱水反应能继续让上述化合物发生脱水反应,形成α,β-不饱和羰基化合物,以上两步反应即熟知的:羟醛缩和反应。当亲核基团替代为烯烃或炔烃进攻羰基,称为:Prins反应,该反应产物因不同反应条件与底物而改变。


